二、填空题(本小题共4题,共23分)
17.在宏观、微观和符号之间建立联系是化学学科的特点.
现有A、B、C、D四种物质,其微观示意图见下表.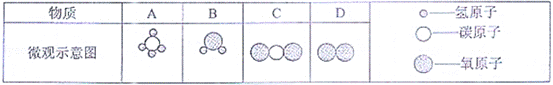
(1)B物质相对分子质量为 18 ;
(2)上述物质中属于单质的是 D (填物质序号)属于有机物的是 CH4 (填写化学式)
(3)一个C分子是由 两个氧原子和一个碳原子 构成的;
(4)写出反应A+D→B+C的化学方程式: CH4+2O2 CO2+2H2O .
CO2+2H2O .
考点: 微粒观点及模型图的应用;单质和化合物的判别;有机物与无机物的区别;相对分子质量的概念及其计算;书写化学方程式、文字表达式、电离方程式。
专题: 微观粒子模拟图型。
分析: 根据物质的微观结构图分子各分子的结构,并根据结构写出ABCD代表的物质化学式,然后进行分析判断即可;
解答: 解:由ABCD四种物质的分子结构可知它们分别是:CH4、H2O、CO2、O2,据此解答下题:
(1)B是水,其相对分子质量等于1×2+16=18;
(2)单质是由同种元素组成的纯净物,所以O2是单质,含碳的化合物是有机物(一氧化碳、二氧化碳和碳酸盐除外),所以CH4属于有机物.
(3)C分子是二氧化碳的分子,其结构是每两个氧原子和一个碳原子构成一个二氧化碳分子.
(4)依据ABCD的化学式可知A+D→B+C的化学方程式为:CH4+2O2 CO2+2H2O;
CO2+2H2O;
故答案为:(1)18;(2)D;CH4;(3)两个氧原子和一个碳原子.(4)CH4+2O2 CO2+2H2O;
CO2+2H2O;
点评: 本题考查了微观示意图表示的化学反应以及物质化学式的确定,完成此题,可以依据图示以及质量守恒定律进行.
18.环境污染、食品安全问题总是时有发生,毒胶囊事件是指一些企业用皮革废料熬制成的工业明胶制成药用胶囊,最终流入药品企业,进入患者腹中,由于皮革在加工时要使用含铬的鞣制剂,因此这样制成的胶囊,往往重金属铬超标.高价态铬对人体的毒性非常强,对肝、肾等内脏器官和DNA造成损伤,在人体内蓄积具有致癌性并可能诱发基因突变.常见的重铬酸钾(K2Cr2O7)为橙红色晶体,溶于水,不溶于乙醇,加热时能分解.与有机物接触摩擦,撞击能引起燃烧.与还原剂(如酒精)反应生成三价铬离子(根据这一原理,交警可以现场检查司机是否酒后驾车).
根据以上信息,回答下列问题:
(1)“往往重金属铬超标”中的“铬”是指 B (填序号)A、铬金属单质 B、铬元素
(2)K2Cr2O7中各元素的质量比为:K:Cr:O= 39:52:56 ;
(3)以上描述中,属于K2Cr2O7的化学性质的是(写两点): 加热时能分解 、 与有机物接触摩擦,撞击能引起燃烧.(与还原剂(如酒精)反应生成三价铬离子) ;
(4)铬有多种价态,K2Cr2O7中铬元素的化合价为 +6价 ,写出金属铬在空气中加热生成+3价的铬的氧化物的化学方程式 4Cr+3O2 2Cr2O3 .
2Cr2O3 .
考点: 亚硝酸钠、甲醛等化学品的性质与人体健康;元素的概念;有关元素化合价的计算;元素质量比的计算;化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式。
专题: 化学与生活健康。
分析: (1)根据表示一类原子的总称考虑;(2)根据元素质量计算方法考虑;(3)根据化学性质是通过化学变化表现出来的性质;(4)根据化合价的计算和方程式的书写方法考虑.
解答: 解:(1)“往往重金属铬超标”中的“铬”是指铬这一类原子的总称,具有相同核电荷数的一类原子的总称属于元素,所以指的元素;
(2)K2Cr2O7中各元素的质量比为:K:Cr:O=39×2:52×2:16×7=39:52:56;
(3)加热时能分解.与有机物接触摩擦,撞击能引起燃烧.与还原剂(如酒精)反应生成三价铬离子都是通过化学变化表现出来的,属于化学性质;
(4)设铬元素的化合价为X则:(+1)×2+X×2+(﹣2)×7=0解得X=+6;反应物是铬和氧气,生成物是三氧化二铬,用最小公倍数法配平,反应条件是加热.
故答案为:(1)B;(2)39:52:56;(3)加热时能分解;与有机物接触摩擦,撞击能引起燃烧.(与还原剂(如酒精)反应生成三价铬离子);
(4)+6价;4Cr+3O2 2Cr2O3
2Cr2O3
点评: 解答本题关键是要知道元素质量的计算,化合价的计算,化学方程式的书写,掌握化学性质的判断方法.
19.化学与生活息息相关,请用学过的化学知识解决下列问题.
(1)下列食物富含蛋白质的是 A (填字母序号,下同);富含维生素的是 B .
(2)硬水给生活和生产带来很多麻烦,生活中可用 肥皂水 来区别硬水和软水,常用 加热煮沸 的方法来降低水的硬度.
(3)学习化学可以帮助我们解决许多生活中的问题,请你根据灭火原理作一扑灭森林火灾的预案:你用的灭火方法是(这里只要求写一种): 砍伐树木形成隔离带 ,这一灭火的原理是 隔离可燃物 .
考点: 食品、药品与健康食品中的有机营养素;硬水与软水;灭火的原理和方法。
专题: 化学与生活健康。
分析: (1)根据常见物质中含有的营养成分考虑;(2)根据硬水与软水的鉴别方法和转化方法考虑;(3)根据灭火的方法考虑.
解答: 解:(1)鱼中富含有蛋白质,苹果中富含有维生素,饼干中富含有糖类;玉米油中富含有油脂;
(2)用肥皂水可以鉴别硬水和软水,泡沫多的是软水,泡沫少的是硬水,硬水软化的方法是蒸馏或煮沸,常用的方法是加热煮沸;
(3)灭火的方法有:隔绝空气、降低温度到可燃物着火点以下、隔离可燃物;扑灭森林火灾一般用砍伐树木形成隔离带,主要是隔离可燃物.
故答案为:(1)A;B;(2)肥皂水;加热煮沸;(3)砍伐树木形成隔离带;隔离可燃物.
点评: 解答本题的关键是要知道常见物质中的营养成分,知道硬水、软水的鉴别和转化,了解灭火的方法和原理.
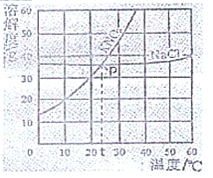
20.如图为硝酸钾和氯化钠的溶解度曲线,结合图形回答下列问题
(1)图中P的含义是 t℃时,硝酸钾和氯化钠的溶解度相等 .
(2)10℃时,向100g水中加入30g硝酸钾,此时溶液是否饱和 是 (填“是”或者“否”).若此基础上再加入10g硝酸钾,为使硝酸钾完全溶解,可以采用的方法是 升高温度 .
(3)当氯化钠饱和溶液中有少量的硝酸钾可用下列 A 法提纯氯化钠(填字母序号)
A、蒸发结晶 B、冷却热饱和溶液 C、趁热过滤.
考点: 固体溶解度曲线及其作用;结晶的原理、方法及其应用;饱和溶液和不饱和溶液;饱和溶液和不饱和溶液相互转变的方法。
专题: 溶液、浊液与溶解度。
分析: (1)根据曲线中交点的含义考虑;(2)根据10℃时,硝酸钾的溶解度进行计算;(3)根据氯化钠的溶解度受温度的影响大小考虑.
解答: 解:(1)曲线中交点表示该温度时两种物质的溶解度相等,所以图中P的含义是t℃时,硝酸钾和氯化钠的溶解度相等;
(2)10℃时,硝酸钾的溶解度是20g,即该温度下100g水中最多溶解20g硝酸钾;所以10℃时,向100g水中加入30g硝酸钾,此时溶液是饱和溶液,且有10g没溶解;若此基础上再加入10g硝酸钾,为使硝酸钾完全溶解就要升高温度,增大硝酸钾的溶解度;
(3)如果溶解度受温度影响较大的物质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂.因为氯化钠的溶解度受温度影响不大,就要用蒸发溶剂的方法.
故答案为:(1)t℃时,硝酸钾和氯化钠的溶解度相等;(2)是;升高温度;(3)A..
点评: 解答本题的关键是要知道溶解度的四要素:一定温度、100g溶剂、饱和状态、溶解的质量;知道交点的含义;溶质从溶液中结晶析出的方法.
三、实验题(本小题共2小题,共23分)
21.以下是初中化学的一些基本实验: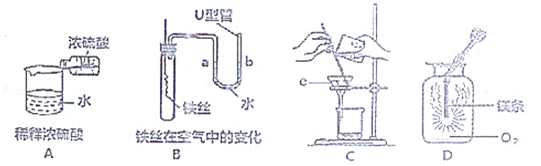
(1)A中的操作中有一个明显的错误,请指出来: 没有用玻璃棒搅拌 ;
(2)一段时间后,B中的实验现象为 铁丝表面变红,U型管中a液面上升,b液面下降 ;
(3)C的实验操作的名称是 过滤 ;写出标号c的仪器名称: 漏斗 ;用C的实验操作可以完成的实验是 ③
①从NaCl溶液中得到NaCl晶体 ②除去Na2CO3溶液中混有的KCl ③将CaCO3与水分离
(4)D中发生反应的化学方程式为 2Mg+O2 2MgO .
2MgO .
考点: 浓硫酸的性质及浓硫酸的稀释;过滤的原理、方法及其应用;金属锈蚀的条件及其防护;书写化学方程式、文字表达式、电离方程式。
专题: 实验性简答题。
分析: (1)根据浓硫酸的稀释方法进行分析解答.
(2)根据铁生锈的原理进行分析解答.
(3)根据过滤操作的原理、方法、注意事项等进行分析解答.
(4)D实验是镁在氧气中燃烧,写出反应的化学方程式即可.
解答: 解:(1)稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中没有用玻璃棒搅拌.
(2)铁生锈的两个条件是有水和空气,一段时间后,铁丝生锈变红,消耗掉试管内的氧气,试管内气体压强变小,U型管中水被外界大气压压入,所以a液面上升,b液面下降.
(3)C的实验操作的名称是过滤;标号c的仪器名称是漏斗;过滤是将不溶于水的固体与液体分离的一种方法,①从NaCl溶液中得到NaCl晶体可以采用蒸发结晶的方法;②Na2CO3、KCl均易溶于水,不能用过滤的方法分离;CaCO3不溶于水,可用过滤的方法与水分离.
(4)镁在氧气中燃烧生成氧化镁,反应的化学方程式为:2Mg+O2 2MgO.
2MgO.
故答案为:(1)没有用玻璃棒搅拌;(2)铁丝表面变红,U型管中a液面上升,b液面下降;(3)过滤;漏斗;③;(4)2Mg+O2 2MgO.
2MgO.
点评: 本题难度不大,掌握浓硫酸的稀释、铁生锈的原理、过滤操作、化学方程式的书写等是正确解答本题的关键.
22.某实验小组用图A完成课本实验“碳酸氢钠与盐酸反应的探究”后,他们发现两种反应物的用量不同时反应后溶液中的成分也可能不同,于是他们对碳酸氢钠与盐酸反应后的大试管中溶液的成分进行探究,请回答以下问题:
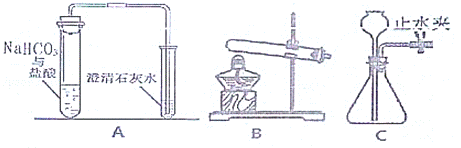
(1)写出图A中大试管发生反应的化学方程式: NaHCO3+HCl═NaCl+H2O+CO2↑ ;
写出小试管中发生反应的化学方程式: Ca(OH)2+CO2=CaCO3↓+H2O ;
(2)若实验室制二氧化碳应选装置 C (填B或C),药品为: 稀盐酸和石灰石 (填名称):
【提出假设】小组成员认为A中大试管的溶液的溶质只能存在三种情况:
假设1.两溶液恰好完全反应,溶质为NaCl;
假设2.两溶液完全反应后,盐酸过量,溶质为NaCl和HCl;
假设3. 两溶液完全反应后,碳酸氢钠过量,溶质为NaCl和NaHCO3 .
【设计并进行实验和得出结论】小组同学讨论后发现只要用反应物本身两种试剂(碳酸氢钠溶液和稀盐酸)就可以完成实验,请填写下表中的实验内容:
实验 | 实验操作 | 实验现象 | 实验结论 |
① | 取反应后的溶液少量于试管1中,加入过量的 碳酸氢钠溶液 | 有 气泡冒出 | 溶液中存在 盐酸 假设 ② 成立 |
② | 取反应后的溶液少量于试管2中,加入过量的 稀盐酸 | 有 气泡冒出 | 溶液中存在 碳酸氢钠 假设 ③ 成立 |
③ | 综合实验①和实验②两个实验操作,发现都没有明显的实验现象 | 溶液中只存在NaCl,假设1成立 | |
考点: 实验探究物质的组成成分以及含量;二氧化碳的实验室制法;酸的化学性质;碳酸钠、碳酸氢钠与碳酸钙;常见离子的检验方法及现象;书写化学方程式、文字表达式、电离方程式。
专题: 科学探究。
分析: (1)根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳以及二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行解答;
(2)根据实验室是用稀盐酸和石灰石反应制取二氧化碳,反应物的状态为固体和液体,反应条件不需要加热进行解答;
【提出假设】:根据碳酸氢钠过量进行解答;
【设计并进行实验和得出结论】:根据碳酸氢钠和盐酸反应放出二氧化碳气体进行解答.
解答: 解:(1)碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式:NaHCO3+HCl═NaCl+H2O+CO2↑;二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O;
(2)实验室是用稀盐酸和石灰石反应制取二氧化碳,反应物的状态为固体和液体,反应条件不需要加热,所以制二氧化碳应选装置应选C;
【提出假设】:假设碳酸氢钠过量,两溶液完全反应后,碳酸氢钠过量,溶质为NaCl和NaHCO3;
【设计并进行实验和得出结论】:根据碳酸氢钠和盐酸反应放出二氧化碳气体,可以利用这一现象进行实验.
故答案为:(1)NaHCO3+HCl═NaCl+H2O+CO2↑;Ca(OH)2+CO2=CaCO3↓+H2O;
(2)C;稀盐酸和石灰石;
【提出假设】:两溶液完全反应后,碳酸氢钠过量,溶质为NaCl和NaHCO3;
【设计并进行实验和得出结论】:碳酸氢钠溶液;气泡冒出;盐酸;②;稀盐酸;气泡冒出;碳酸氢钠;③.
点评: 重点考查了碳酸氢钠的性质、方程式的书写以及实验室中常见气体的制备等知识,比较综合.
四、计算题(本题共有1小题,共6分)
23.工业上用煅烧石灰石(主要成分为CaCO3)制取生石灰,其生产流程图如下:
(1)某工厂用12t含碳酸钙为75%的石灰石,其中所含碳酸钙的质量是 9 t.
(2)上述石灰石理论上可以制得生石灰多少t?(写出计算过程)
考点: 含杂质物质的化学反应的有关计算。
专题: 有关化学方程式的计算。
分析: (1)根据碳酸钙的含量进行解答.
(1)可根据第一问碳酸钙的质量,利用碳酸钙分解的化学方程式进行解答.
解答: 解:(1)碳酸钙的质量=12t×75%=9t;
故填:9;
(2)设生成氧化钙的质量为x.则
CaCO3 CaO+CO2↑
CaO+CO2↑
100 56
9t x
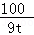 =
=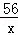 ,
,
解之得:x=5.04t
因为生成的生石灰中含有未参与反应的杂质,杂质的质量=12t×(1﹣75%)=3t
所以最终可以生产生石灰的质量=5.04t+3t=8.04t
答:可生产生石灰8.04t.
点评: 本题主要考查了学生解决有关含杂质物质的化学反应的计算的能力,解题关键是求反应后物质的质量时,既要考虑生成的物质,又要考虑原混合物中没有参加反应的物质.











