一、选择题(本题共10个小题,每小题2分,共20分。每小题只有一个选项符合题意,将符合题意的选项字母填入括号内)
1.生产生活中的下列变化,属于化学变化的是 ( )
A.冰块融化 B.海水晒盐 C.铁锅生锈 D.酒精挥发
【答案】C
【解析】A、冰块融化是指水由固态变为了液态的水,并没有产生新的物质,故A属于物理变化;B、海水晒盐是指通过蒸发的方法,将海水中的水分蒸发掉,而使溶解在海水中的氯化钠析出的过程,该过程中并没有产生新的物质,故B属于物理变化;C、铁锅生锈是指铁和氧气及水反应生成了铁锈,铁锈的主要成分为氧化铁,即该过程中产生了新的物质,故C属于化学变化;D、酒精挥发只是酒精由液态变成了气态,并没有产生新的物质,故D属于物理变化,故选C。
2.2012年4月15日,央视曝光河北一些企业生产的药用胶囊里重金属铬(Cr)超标,即震惊全国的“毒胶囊”事件。已知铬原子核内有24个质子,铬元素的相对原子质量为52。下列有关 铬元素的说法中不正确的是 ( )
铬元素的说法中不正确的是 ( )
A.铬原子的核外电子数为24 B.铬元素的原子序数是52
C.铬原子核由质子和中子构成 D.铬原子呈电中性

3.下列关于碳单质的说法中正确的是 ( )
A.C60的相对分子质量为720
B.金刚石、石墨和C60都由碳元素组成,结构相同
C.木炭具有还原性,常温下可以将氧化铜中的铜还原出来
D.石墨很软,不能用于制石墨电极
【答案】A
【解析】本题主要考查碳元素组成的单质的种类、结构、性质及用途。A、C60的相对分子质量为:12×60 =720,故A正确;B、金刚石、石墨和C60都由碳元素组成的,结构不同,物理性质不同,故B错误;C、木炭具有还原性,高温下可以将氧化铜中的铜还原出来,故C错误;D、石墨有良好的导电性,可用于制石墨电极,故D错误,故选A。
=720,故A正确;B、金刚石、石墨和C60都由碳元素组成的,结构不同,物理性质不同,故B错误;C、木炭具有还原性,高温下可以将氧化铜中的铜还原出来,故C错误;D、石墨有良好的导电性,可用于制石墨电极,故D错误,故选A。
4.下列衣物所使用的主要材料属于合成纤维的是 ( )

【答案】C
【解析】本题主要考查学生对天然纤维与合成纤维的特点的认识和区别能力。A、纯棉夹克是由棉花制成的,棉花属天然纤维,故错误;B、羊绒围巾是有羊毛制成的,羊毛属于天然纤维,故错误;C、腈纶上衣是由腈纶制成的,腈纶是聚丙烯腈纤维,属于合成纤维,故正确;D、丝绸是蚕丝制成的,蚕丝属于天然纤维,故错误,故选C。
5.下列化学方程式书写正确的是 ( )
A.2Fe+6HCl=2FeCl3+3H2↑ B.CO+Fe2O3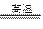 2Fe+CO2
2Fe+CO2
C.2NaOH+CuSO4=Na2SO4+Cu(OH)2 D.NaHCO3+HCl=NaCl+CO2↑+H2O
【答案】D
【解析】A、铁在和盐酸反应生成的是氯化亚铁(F eCl2)而不是氯化铁(Fe
eCl2)而不是氯化铁(Fe Cl3),故A书写错误;B、一氧化碳和氧化铁反应的化学方程式为:3CO+Fe2O3
Cl3),故A书写错误;B、一氧化碳和氧化铁反应的化学方程式为:3CO+Fe2O3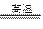 2Fe+3CO2,而题中的化学方程式没有配平,故B书写错误;C、氢氧化钠和硫酸铜反应生成了氢氧化铜[Cu(OH)2]沉淀,而题中没加沉淀符号,故C书写错误;D、碳酸氢钠和盐酸反应生成了氯化钠、水和二氧化碳,其化学方程式为:NaHCO3+HCl═NaCl+CO2↑+H2O,故D书写正确,故选D。
2Fe+3CO2,而题中的化学方程式没有配平,故B书写错误;C、氢氧化钠和硫酸铜反应生成了氢氧化铜[Cu(OH)2]沉淀,而题中没加沉淀符号,故C书写错误;D、碳酸氢钠和盐酸反应生成了氯化钠、水和二氧化碳,其化学方程式为:NaHCO3+HCl═NaCl+CO2↑+H2O,故D书写正确,故选D。
6.下列说法中正确的是 ( )
A.pH<7的雨水叫酸雨 B.pH<7的溶液,pH越小,酸性越弱
C.使酚酞溶液变红的溶液是碱性溶液 D.使用pH 试纸应先用蒸馏水润湿
试纸应先用蒸馏水润湿
【答案】C
【解析】A、pH<5.6的雨水称为酸雨,故A错误;B、pH<7的溶液,pH越小,酸性越强,故B错误;
C、使酚酞溶液变红的溶液是碱性溶液,故C正确;D、使用PH试纸先用蒸馏水润湿,相当于稀释了被测液的酸碱性,故D错误;故选C。
7.下列对有关物质的分类不正确的是  ( )
( )
选项 | 物质 | 分类 | 不同类物质 |
A | 干冰、白酒、加碘盐、食醋 | 混合物 | 干冰 |
B | CaO、H2O、P2O5、K2CO3 | 氧化物 | H2O |
C | HgO、NaOH、KCl、P4(白磷) | 化合物 | P4(白磷) |
D | 甲烷、乙醇、硝酸钾、葡萄糖 | 有机物 | 硝酸钾 |
【答案】B
【解析】本题考查物质分类的 知识。A、白酒、加碘盐、食醋均是由多种物质混合而成的,均属于混合物;干冰是固态的二氧化碳,只含有一种物质,属于纯净物;故物质的分类正确;B、CaO、H2O、P2O5均是由两种元素组成且有一种是氧元素,均属于氧化物;K2CO3而是由钾、碳、氧三种元素组成的化合物,不属于氧化物;故物质的分类错误.
知识。A、白酒、加碘盐、食醋均是由多种物质混合而成的,均属于混合物;干冰是固态的二氧化碳,只含有一种物质,属于纯净物;故物质的分类正确;B、CaO、H2O、P2O5均是由两种元素组成且有一种是氧元素,均属于氧化物;K2CO3而是由钾、碳、氧三种元素组成的化合物,不属于氧化物;故物质的分类错误.
C、HgO、NaOH、KCl均是由不同种元素组成的纯净物,均属于化合物;而P4(白磷)是由一种元素组成的纯净物,属于单质;故物质的分类正确;D、甲烷、乙醇、葡萄糖均是含碳元素的化合物,均属于有机物;硝酸钾不含碳元素,属于无机物;故物质的分类正确,故选B。
8.配制100g质量分数为10%的氢氧化钠溶液,称量氢氧化钠固体时除使用托盘天平(带砝码)和药匙外,还需要用到下列仪器中的 ( )
A.玻璃棒 B.烧杯 C.100 mL量筒  D.胶头滴管
D.胶头滴管
【答案】B
【解析】由于氢氧化钠具有腐蚀性,不能直接放在天平上或纸上,应该放在玻璃器皿中称量,所以还要用到烧杯,故选B。
9.先取甲、乙、丙、丁四种金属粉末,分别投入相同浓度的稀盐酸中,只有甲、乙能产生气体,乙反应更剧烈;再取一小块丁投入丙的硝酸盐溶液中,丁的表面有丙析出。则甲、乙、丙、丁四种金属的活动性顺序为 ( )
A.甲>乙>丙>丁 B.乙>甲>丙>丁 C.丁>丙>乙>甲 D.乙>甲>丁>丙
【答案】D
【解析】本题考查了金属活动性顺序的应用,在金属活动性顺序中,氢前的金属能与酸发生置换反应,且位置越靠前,反应越剧烈;位置在前的金属能把位于其后的金属从其盐溶液中置换出来,由题意可知:将这四种金属粉末分别投入相同浓度的盐酸中,只有甲、乙发生反应并产生气泡,而且乙反应更剧烈,说明甲和乙排在氢前,且乙在甲的前面,丙、丁排在氢后.将丁投入丙的硝酸盐溶液中,丁的表面有丙析出,说明丁在丙的前面.所以,四种金属的活动性顺序为:乙>甲>丁>丙,故选D。
10.一定条件下,下列物质在密闭容器内反应一段时间,测得反应产前后各物质的质量如下:
物质 | X | Y | Z | W |
反应前质量/g | 10 | 2.2 | 16.2 | 0.9 |
反应后质量/g | a | 4.4 | 8.1 | 1.8 |
根据上表信息判断,下列说法中不正确的是 ( )
A.X、Z是反应物,Y、W是生成物 B.a=15
C.反应中Y、W两种物质变化的质量比为22︰9 D.Z为化合物
 10+2.2+16.2+0.9=a+4.4+8.1+1.8,故a=15克,根据反应物反应后质量减少,生成物质量增加则可推测反应物为Z;生成物为X、Y、W;A、由以上推测可知,反应物为Z;生成物为X、Y、W,故A错误;B、a=15,故B正确;C、反应中Y、W两种物质变化的质量比为(4.4-2.2):(1.8-0.9)=22:9,故C正确;D、从以上推测可以看出,该反应为Z物质分解为XYW三种物质,故Z为化合物说法正确,故D正确,故选A。
10+2.2+16.2+0.9=a+4.4+8.1+1.8,故a=15克,根据反应物反应后质量减少,生成物质量增加则可推测反应物为Z;生成物为X、Y、W;A、由以上推测可知,反应物为Z;生成物为X、Y、W,故A错误;B、a=15,故B正确;C、反应中Y、W两种物质变化的质量比为(4.4-2.2):(1.8-0.9)=22:9,故C正确;D、从以上推测可以看出,该反应为Z物质分解为XYW三种物质,故Z为化合物说法正确,故D正确,故选A。
二、填空题(本题共3个小题,共22分)
11.(6分)用化学用语填空:
(1)银 ;(2) 4个二氧化硫分子 ;(3)2个铝离子 ;
(4)高锰酸钾  ;(5)+5价的氮元素 ;
;(5)+5价的氮元素 ;
(6)由Ca2+和H2PO4— 构成的磷酸二氢钙  。
。
【答案】(1)Ag;(2) 4SO2;(3)2Al3+(4)KMnO4;(5) 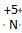 ;
;
(6)由Ca(H2PO4)2。
【解析】本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的是物质、分子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义;并能根据物质化学式的书写规则正确书写物质的化学式。(1)银由原子构成,其化学式用元素符号表示为:Ag;(2)首先写出二氧化硫的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以4个二氧化硫分子表示为:4SO2;(3)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后;若表示多个该离子,就在其元素符号前加上相应的数字,2个铝离子即2Al3+;(4)高锰酸钾由锰元素、钾元素和氧元素组成,其化学 式是:KMnO4;(5)元素化合价的表示方法:在该元素的上方用正负号和数字表示,正负号在前,数字在后,所以+5价的氮元素可表示为:
式是:KMnO4;(5)元素化合价的表示方法:在该元素的上方用正负号和数字表示,正负号在前,数字在后,所以+5价的氮元素可表示为: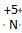 (6)书写物质的化学式时,正价在前,负价在后,然后交叉化合价数值,写出物质的化学式,所以磷酸二氢钙的化学式是Ca(H2PO4)2。
(6)书写物质的化学式时,正价在前,负价在后,然后交叉化合价数值,写出物质的化学式,所以磷酸二氢钙的化学式是Ca(H2PO4)2。
12.(8分) 常用仪器的使用、常见气体的制取是初中化学实验的基础内容。请根据下列实验装置回答问题。
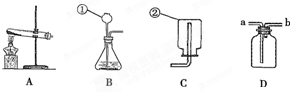
(1) 写出上图中部分仪器的名称:① ;② 。
(2) 使用A装置制取气体,对反应物状态的要求是 。
(3) 用C装置可以收集O2、CH4、NH3、Cl2中的 (填化学式)。
(4) 实验室制取二氧化碳气体,组装好实验装置后,应进行的必要操作是 ;若用D装置收集二氧化碳气体, 应从 (填“a”或“b”)通入气体。
【答案】 (1)①长颈漏斗②集气瓶 (2)固体 (3) CH4、NH3 (4)检查装置的气密性,a。
【解析】(1)图中仪器是长颈漏斗、集气瓶;(2)A装置适用于加热固体制取气体;(3)O2、CH4、NH3、Cl2的相对分子质量分别是:32、16、17、71,所以O2、Cl2可用向上排空气法收集,CH4、NH3可用向下排空气法收集;(4)连接装置后要检查装置的气密性,气密性良好,才能加入药品制取气体;二氧化碳的密度比空气大,所以应从a端通入气体。
13.(8分)根据图1、图2中三种固体物质的溶解度曲线回答问题。
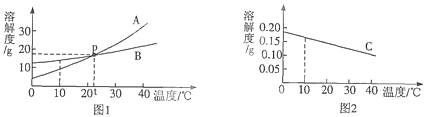
(1)分析图1,P点处A、B两种物质的溶解度关系是A B(填“>”、“<”或“=”);取一定质量的A的饱和溶液,将溶液温度从t℃降低到10℃,溶液中溶质的质量分数 (填“增大”、“减小”或“不变”)。
(2)分析图2,要使C的饱和溶液变成不饱和溶液,可采用的方法是:
① ;② 。
(3)10℃时,A、B、C的饱和溶液中溶质的质量分数由大到小的顺序是 。
【答案】(1)=;减少(2)降低温度或加溶剂水(3)B>A>C
【解析】(1)P点处A、B两种物质相交于一点,故其溶解度关系是A=B;A的溶解度随温度的降低而减小,将溶液温度从t℃降低到10℃,要析出溶质,仍为饱和溶液;饱和溶液中溶质的质量分数的计算式:溶解度/(溶解度+100g)×100%,即溶解度越大质量分数也就越大,所以降温后溶液中溶质的质量分数减小;(2)观察图2可知:C物质的溶解度随温度的升高而减小,所以,要使C的饱和溶液变成不饱和溶液,可采用的方法是增加溶剂、升高温度;(3)10℃时,A、B、C的溶解度大小顺序是B>A>C,由(1)所得结论:溶解度越大质量分数也就越大,所以10℃时,A、B、C的饱和溶液中溶质的质量分数由大到小的顺序是B>A>C。











